一、VR教學(xué)目標(biāo)
1、知識與技能
(1)了解物質(zhì)的量及其單位,了解物質(zhì)的量與微觀粒子數(shù)之間的關(guān)系;
(2)通過對1 mol物質(zhì)質(zhì)量的討論,理解摩爾質(zhì)量的概念以及摩爾質(zhì)量和相對原子質(zhì)量、相對分子質(zhì)量之間的關(guān)系。
2、過程與方法
(1)通過對物質(zhì)的量概念的理解,嘗試從定量的角度去認(rèn)識物質(zhì),體會定量研究方法對研究和學(xué)習(xí)化學(xué)的重要作用;
(2)經(jīng)歷物質(zhì)的量與微觀粒子數(shù)、物質(zhì)的質(zhì)量之間的換算,理解概念、運(yùn)用和鞏固概念,提高化學(xué)計算能力。
3、情感態(tài)度與價值觀
在物質(zhì)的量概念的建構(gòu)過程中感受到微觀和宏觀的相互轉(zhuǎn)化是研究化學(xué)的科學(xué)方法之一。
二、教學(xué)重點(diǎn)與難點(diǎn)
1、教學(xué)重點(diǎn)
(1)物質(zhì)的量及其單位、阿伏加德羅常數(shù);
(2)摩爾質(zhì)量概念和有關(guān)摩爾質(zhì)量的計算。
2、教學(xué)難點(diǎn)
(1)物質(zhì)的量概念的教學(xué);
(2)摩爾質(zhì)量、氣體摩爾體積概念的建立。
三、VR教學(xué)過程
【教師】大家都知道曹沖稱象的故事,那么,曹沖稱象的主要思想是什么呢?將巨大的不可直接稱重的大象“分解”成一塊塊可以稱重的石頭。這個故事給我們的啟示就是化整為零。日常生活中,買大米時我們一般論斤買而論“粒”就不方便,一斤就是許多“粒”的集合;買礦泉水我們可以論瓶買,但買多的也可以論箱買,一箱就是24瓶的集合等等。一滴水中就大約含有1.7萬億億個水分子,如果一個個去數(shù),即使分秒不停,一個人窮其一生也無法完成這個工作。那我們怎樣才能既科學(xué)又方便地知道一定量水中含有多少個水分子呢?所以,這里需要一個“橋梁”,需要一個物理量把宏觀質(zhì)量和微觀粒子數(shù)聯(lián)系起來,這個物理量就是“物質(zhì)的量”。
第14屆國際計量大會通過以“物質(zhì)的量”作為化學(xué)計量的基本單位量,至此,物質(zhì)的量和長度、質(zhì)量、時間等成為國際單位制中的7個基本單位。
物理量 | 單位名稱 | 單位符號 |
長度 | 米 | m |
質(zhì)量 | 千克(公斤) | kg |
時間 | 秒 | S |
電流 | 安[培] | A |
熱力學(xué)溫度 | 開[爾文] | K |
物質(zhì)的量 | 摩[爾] | mol |
發(fā)光強(qiáng)度 | 坎[德拉] | cd |
【學(xué)生】理解國際基本單位。
【教師】強(qiáng)調(diào):1、物質(zhì)的量表示物質(zhì)所含微粒的多少,這四個字是一個整體,不得簡化或增添任何字,物質(zhì)的量實(shí)際上表示含有一定數(shù)目粒子的集體。
2、物質(zhì)的量是以微觀粒子為計量的對象,而這里的“粒子”是指構(gòu)成物質(zhì)的“基本單元”、這個基本單元可以是分子、原子、離子、中子、質(zhì)子等單一粒子,也可以是這些粒子的特定組合。
3、物質(zhì)的量用符號“n”表示。
觀看VR互動教學(xué)視頻-摩爾的概念,提問每種物理量都有相應(yīng)的單位。速率的單位是“米/秒”,“物質(zhì)的質(zhì)量”的單位是“千克”等。“物質(zhì)的量”作為一種物理量也應(yīng)有相應(yīng)的單位,它的單位是什么?科學(xué)上用“摩爾”作為“物質(zhì)的量”的單位。1摩爾是多少?


【學(xué)生】在國際上摩爾這個單位是以0.012 kg 12C 中所含的原子數(shù)目為標(biāo)準(zhǔn)的,即1 mol粒子集體所含的粒子數(shù)與0.012 kg 12C 中所含的原子數(shù)相同,約為6.02 × 1023個。也就是說,如果在一定量的粒子集體中所含有的粒子數(shù)與12 g 12C中所含的碳原子數(shù)目相同,則它的物質(zhì)的量為1 mol,而這個數(shù)值(粒子數(shù))我們就叫它為阿伏加德羅常數(shù)。
【教師】已知:一個碳原子的質(zhì)量為 1.993 × 10-23 g 求: 12 g 12C 中所含的碳原子數(shù)。
【學(xué)生】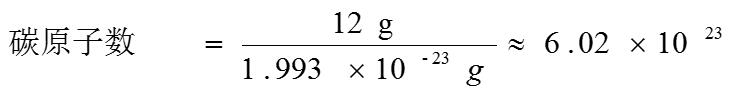
【教師】根據(jù)表中已知條件進(jìn)行計算,將結(jié)果填入表中空格內(nèi):
物質(zhì)微粒 | 物質(zhì)質(zhì)量 | 1個微粒實(shí)際質(zhì)量 | 所含微粒數(shù)目 | 物質(zhì)的量 |
12C | 12 g | 1.993 3 × 10-23 g | 6.02 × 1023 | 1 mol |
Fe | 56 g | 9.3 × 10-23 g | 6.02 × 1023 | 1 mol |
O2 | 32 g | 5.32 ×10-23 g | 6.02 × 1023 | 1 mol |
Na+ | 23 g | 3.82 × 10-23 g | 6.02 × 1023 | 1 mol |
觀看VR互動教學(xué)視頻-摩爾的概念,據(jù)表結(jié)合視頻可得出什么結(jié)論?


【學(xué)生】1 mol 任何粒子集合體都約為 6.02 × 1023 個粒子;而 1 mol 任何粒子或物質(zhì)的質(zhì)量以克為單位時,其數(shù)值都與該粒子的相對原子質(zhì)量相等。
四、板書設(shè)計
第二節(jié) 化學(xué)計量在實(shí)驗中的應(yīng)用
一、物質(zhì)的量的單位——摩爾
1、物質(zhì)的量是一個物理量,表示含有一定數(shù)目粒子的集合體。
注意:1. 是七個國際基本物理量之一。
2. 是一個專有名詞,由固定字?jǐn)?shù)組成,不能分割、不能增減。
3. 符號為“n”。
4. 微粒是指:分子、原子、離子、電子、質(zhì)子、原子團(tuán)、中子等。
5. 粒子必須十分明確,且用化學(xué)式表示。
2、摩爾
(1)概念:是物質(zhì)的量的單位,簡稱摩。
(2)符號:mol 。
3、阿伏伽德羅常數(shù)(NA):把1 mol任何粒子的粒子數(shù)叫做阿伏加德羅常數(shù),數(shù)值為6.02×1023/mol。
4、物質(zhì)的量、阿伏加德羅常數(shù)與粒子數(shù)( N )之間的關(guān)系:
n =N/NA
5、摩爾質(zhì)量
(1)概念:單位物質(zhì)的量的物質(zhì)所具有的質(zhì)量叫做摩爾質(zhì)量。
(2)符號:M
(3)單位:g ? mol -1或 g / mol 。
(4)物質(zhì)的量、質(zhì)量和摩爾質(zhì)量之間的關(guān)系:
n =m/M